Für behandelnde Ärztinnen und Ärzte
- Epidemiologie
- Krankheitssymptome
- Pathologie
- Staging und Prognose
- Chirurgische Therapie
- Chemotherapie
- Strahlentherapie
- Multimodale Therapie
- Palliative Therapie
- Relevante Literatur
- Ärztliche Meldung einer Berufskrankheit
Diagnostik und Therapie des malignen Pleuramesothelioms
Prim. Dr. Christian Geltner, Klinikum Klagenfurt
Epidemiologie
Asbest
Asbest gilt heutzutage als der Hauptrisikofaktor zur Entwicklung eines malignen Mesothelioma. Unter dem Begriff Asbest werden verschiedene Minerale mit sehr dünnen Fasern zusammengefasst. Chrysotil, ein Serpentin sowie Crocidolit, Amosit, Anthophyllit, Tremolit und Actinolit aus der Amphibolen Gruppe. Chrysotile ist weniger lang biologisch aktiv und kann nicht sehr lange in der Lunge nachgewiesen werden. Chrysotil, Amosit und Crocidolit wurde reichlich abgebaut und industriell im Schiffsbau, Eisenbahnbau und in der Brandschutztechnik verwendet. Erste Hinweise über die hohe Kanzerogenität gab es in Großbrittanien und Südafrika bereits in den 60er Jahren. Die Inzidenz von Mesotheliomen ohne Asbestkontakt ist extrem niedrig (<1:1 Million). Asbestexposition ist typischerweise Arbeitsabhängig und somit als Berufserkrankung anerkannt. Es gibt nun einen Shift von Asbest-Abbau Arbeitern zu Berufsgruppen, die in der Endfertigung tätig sind, also Elektriker, Installateure, Dämmtechniker, Wärmeschutztechniker u.a. International ist eine Prädominanz des männlichen Geschlechts festzustellen mit einer Verteilung über 80% (typischerweise berufsabhängig).
Mit einer hohen Umweltbelastung durch Asbest müssen Menschen rechnen, die in der Nähe von natürlichen Vorkommen aufwachsen (Türkei, Korsika, Zypern) oder in Gegenden, in denen Asbest zur Weißung von Hauswänden verwendet wurde. Weiters gibt es eine zunehmende Inzidenz von nicht berufsbedingten Asbesterkrankungen bei Hausfrauen und Familienmitgliedern von Asbestarbeitern ebenso wie eine hohe Umweltbelastung in der Nähe von Abbau und Verarbeitungsstätten.
Es ist ein eindeutiger Zusammenhang zwischen Menge der Asbestbelastung und der Häufigkeit von Mesotheliomen gegeben. Auch Menschen mit einer minimalen Belastung können ein malignes Mesotheliom entwickeln. Allerdings kann eine einzelne Faser für das Entstehen eines Mesothelioms genügen. Zwischen Asbestbelastung und Auftreten der ersten Symptome besteht eine mittlere Latenzzeit von bis zu 40 Jahren. In über 99% der Fälle ist eine Latenz von mehr als 15 Jahren beschrieben. Insgesamt scheinen Amosit und Crocidolit eine höhere Kanzerogenität zu haben, obwohl wir zum jetzigen Zeitpunkt eine Mesotheliominduktion der anderen Asbestarten nicht ausschließen können. Die meisten Arbeiter waren mit einer Mischbelastung verschiedener Asbeste belastet. Amphibole waren in den meisten Fällen beteiligt.
Das Auftreten von malignen Mesotheliomem ist unabhängig von anderen Asbestassoziierten Erkrankungen wie die klassische Asbestose der Lunge (interstitielle Lungenerkrankung mit Fibrosierung) und die benignen Pleuraplaques. Es sind sowohl das Auftreten von Pleuraplaques und Mesotheliomen Asbest assoziiert, sodass eine vermeintliche Assoziation besteht, während andere Studien aus Australien keinen Zusammenhang zwischen Plaques und dem vermehrten Auftreten von malignen Mesotheliomen erkennen konnten.
Die Belastung in Räumen mit Asbestbaustoffen wurde zunächst als gefährdend gesehen, die Asbestdosis ist allerdings zumeist in extrem niedrigen und nicht karzinogenen wirkenden Dosen nachweisbar. Es konnten keine gehäuften Fälle von Mesotheliomen nachgewiesen werden.
Die Inzidenz von malignen Mesotheliomen schwankt zwischen 7 pro Million in Japan und 40 pro Million in Australien. In Europa liegt die durchschnittliche Inzidenz bei 20/1 Million Einwohner. Die Häufigkeit ist sehr stark von der Menge an Asbestabbau, Asbestimport und Industrialisierung ab. Der Häufigkeitsgipfel ist in Europa aufgrund der langen Latenzzeit für 2015 bis 2020 zu erwarten.
Nicht-Asbest assoziierte Mesotheliome
Außer Asbest sind andere Substanzen in der Entstehung von Mesotheliomen zumindest als Kofaktoren in Diskussion. Natürlich vorkommende Asbeste (Erionite and Fluredenite)oder künstlich erzeugte Materialien (Keramiken), ionisierende Strahlung und SV-40 Virusinfektionen scheinen in der Pathogenese eine Rolle zu spielen. Eine Mitbeteiligung von Zigarettenrauch ebenso wie bei zahlreichen faserhaltigen Materialen wie Glasfasern und mineralische Dämmwollen ist ausgeschlossen. Genetische Faktoren können in der Entstehung eine Rolle spielen, da sowohl familiäre Häufungen als auch eine höhere Inzidenz bei hoher natürlicher Exposition in der Türkei beschrieben wurden.
Screening
Aktuell ist in den gängigen Guidelines keine generelle Screeningmethode etabliert. Low dose CT hat sich als Screeninguntersuchung aufgrund der geringen Sensitivität in Reihenuntersuchungen von Asbestarbeitern nicht durchgesetzt. PET-CT und MR sind erst in der Diagnose bei Verdacht beziehungsweise bereits aufgetretener Symptomatik notwendig.
Zahlreiche Biomarker wie Osteopontin, Mesothelin-related peptides und soluble mesothelin-related peptid (SMRP) sind in Evaluierung, wobei die Werte der falsch positiven Resultate noch deutlich zu hoch sind, um ein Reihenscreening von Asbest-Kontaktpersonen sinnvoll zu machen.
Diagnostik des MPM
Symptomatik und Klinische Diagnose
Patienten kommen typischerweise mit Symptomen wie Atemnot, Husten und Thoraxschmerzen zur Erstuntersuchung. Die Atemnot ist anfangs oft durch einen Pleuraerguss und später durch eine ausgedehnte Restriktion bei Pleuraverschwartung und Tumormassen im Thoraxraum bedingt. Die Patienten beschreiben die Thoraxschmerzen als diffus, manchmal in die Schulter, den Arm oder den Bauchraum ausstrahlend. Neuropathische Schmerzen entstehen bei Einwachsen des Tumors in die nervalen Strukturen des Plexus brachialis der Intercostalnerven oder der paravertebralen Strukturen.
Typischerweise treten Mesotheliome anfangs nur einseitig auf. Im weiteren Verlauf kann sich der Tumor sowohl auf die andere Seite als auch ins Peritoneum ausbreiten. Im Vergleich zu Bronchuskarzinomen ist eine Fernmetastasierung in extrathorakale Lymphknoten und parenchymatöse Organe sehr selten.
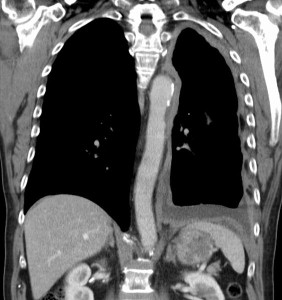
Das Thoraxröntgen zeigt einen Pleuraerguss oder eine pleurale Verdickung. Beides ist nicht diagostisch für ein malignes Mesotheliom. Auch in der ThoraxCT kann ein Mesotheliom nur vermutet aber nicht endgültig diagnostiziert werden. Die Spezifität für pleurale Beteiligungen und Erkrankungen ist sehr hoch, während die Sensivität nur 40% erreicht, da in den meisten Fällen nicht zwischen benignen und malignen Prozessen unterschieden werden kann. Für das weitere Staging ist allerdings sowohl eine CT als auch ein PET-CT sinnvoll. Eine spezifische Diagnostik ist weder in der PET-CT noch in der MR möglich. Für die PET gelten keine klaren SUV-Werte als sensitiv und falsch positive Resultate können bei tuberkulösen Prozessen, parapneumonischen Ergüssen und Urämie auftreten.
Das Häufigste Erstsymptom ist ein Pleuraerguss. Zur Differentialdiagnose der Pleuraergusses siehe dort (Differentialiagnose des PLeurarergusses). Eine Pleurapunktion stellt dort den diagnostischen Standard dar. Ein Pleuramesotheliom sollte nicht allein durch eine zytologische Untersuchung diagnostiziert werden, da die Differentialdiagnose zu pleuralen Metastasen von Bronchus- oder Mammakarzinomen in vielen Fällen nicht getroffen werden kann.
Die Standarduntersuchung zur Diagnose eines Pleuramesothelioms ist die Thorakoskopie. Hierbei kann sowohl eine histologische Probe als auch eine genaue makroskopische Evaluierung der Pleura durchgeführt werden. Die Thorakoskopie kann über einen chirurgischen Zugang (VATS) oder minimal invasiv als medizinische Thorakoskopie in Lokalanästhesie durchgeführt werden. Dies ermöglicht eine Diagnose und Therapie auch in Patienten mit schlechtem Allgemeinzustand.
Alternativ kann eine CT- oder Ultraschall gezielte Feinnadelaspiration oder Stanze durchgeführt werden. Die Sensivität ist hier allerdings deutlich geringer.
Pathologie
Das Pleuramesotheliom geht von der pleuralen Stammzelle aus, die sich einerseits epithelial, anderseits mesenchymal differenziert. Ein Pleuramesotheliom hat daher sowohl epitheliale, als auch sarkomatöse Anteile. Abhängig davon, welche Komponente überwiegt, unterscheidet man 3 Formen:
epithelial (50-70%)
fibrosarkomatös (7-20%)
gemischtförmig (20-35%)
Die pathologische Diagnose und die Differentialdiagnose gestalten sich schwierig. Das Mesotheliom ist ein vielgestaltiger Tumor und andererseits ist die Pleura eine häufige Lokalisation für Metastasen unterschiedlichster Tumorentitäten. Der makroskopische Aspekt kann sich in der Entwicklung des Tumors ändern. Zum einen werden die pathohistologische Merkmale in einer späteren Phase des Tumors klarer, zum anderen zeigen auch sekundäre Neoplasien mesotheliom-ähnliche Bilder (Lymphom, Thymom, Carcinom, u.a.)
| Epithelial | Sarkomatoid | Desmoplastic
Biphasisch ( = mixed) |
| Tubulopapillär Solide Varianten Adenomatoid Kleinzelligzellig Klarzellig Deciduoid Adenoidcystisch Pleomorph Mucin-positive |
Fibrosarcomatoid Chondrosarcomatoid Osteosarcomatoid LeiomyosarcomatoidMalignant fibrous Histiocytom-ähnlichLymphohistiocytoid | Kombinationen aller histomorphologischen Varianten |
Die Charakteristika des malignen Mesothelioms sind in der neuen internationalen Klassifikation von pleuralen Tumoren klar definiert. Die häufigsten in die Pleura metastasierenden Tumoren sind Bronchus-und Mammakarzinome, die in 15% der Fälle mit einem Mesotheliom verwechselt werden können. Auch stark entzündliche Prozesse können in Einzelfällen die Diagnose eines Mesothelioms sehr schwierig machen. In einer französischen Studie (Pathology Group for Assistance in the Diagnosis of Mesothelioma, within the context of the National Program of Mesothelioma Survey 1998–2007) wurden in 13% der Fälle die Erstdiagnose als falsch positiv revidiert.
Die Unterscheidung von epithelialen Mesotheliomen von Adenokarzinomen erfolgt mit Hilfe zahlreicher immunohistochemischer Marker.
Staging und Prognose
Für alle Patienten sind folgende Untersuchungen für Staging und die weitere Therapieplanung erforderlich. Die notwendigen Untersuchungen sind je nach weiterer Therapieoption, sodass im Einzelfall ein dreistufiges Schema in Anlehnung der Expertenempfehlung der ERS von 2010. Eine Basisdiagnostik zur endgültigen Diagnosefindung sollte durchgeführt werden. Je nach Performance Status des Patienten wird weiter entschieden ob eine Therapie in irgendeiner Form möglich ist. In diesem Fall ist ein weiteres Staging auch im Hinblick auf die weitere Diagnose erforderlich.
| Untersuchungen bei Diagnosestellung | |
| Anamnese | Asbestexposition |
| Klinischer Verlauf | Performance Status Symptomatik |
| Physikalische Untersuchung | |
| Radiologie | Thoraxröntgen |
| Blutuntersuchung |
| Untersuchungen zum Staging | |
| Biopsie des Primärtumors | Thorakoskopie Pleurapunktion Feinnadelaspiration |
| Radiologie | CT Schädel MRI/CT bei klinischer Notwendigkeit Knochenscan bei klinischer Notwendigkeit |
| Lungenfunktion |
Für Patienten in jüngerem Alter und mit sehr gutem Performance Status kommt eine multimodale Therapie und eine radikale operative Therapie in Frage. In diesem Fall ist ein sehr exaktes Staging präoperativ erforderlich, um die Operabilität als solche wie auch die funktionelle Fähigkeit eine extrapleurale Pneumektomie mit ausreichender postoperativer Funktion zu überstehen. In diesem Fall sind zahlreiche unterschiedlich möglich, wobei hier international keine Einigkeit besteht. In vielen Konsensusgruppen wurden folgende Untersuchungen empfohlen:
| Untersuchungen präoperativ bei multimodaler Therapie | |
| Lungenfunktion | + BelastungDLCO |
| Primärtumor | Histologische Diagnose |
| Zwerchfell/Pwericardbeteiligung | CT und/oder MRT |
| Fernmetastasen okkult | PET/CT KnochenscanLaparoskopie |
| N2/N3 Beteiligung | VATVAT kontralateralEBUS/EUS TBNAMRT |
Die Prognose des Pleuramesothelioms ist in einer Serie vom Alter, Geschlecht, Tumorstaging und geografischer Region abhängig. Andere Faktoren wie Gewichtsabnahme und Performance Status sind auch bei anderen Tumorentitäten für die Prognose entscheidend ebenso wie Lebensqualität und Symptomenscores. Epitheliale Mesotheliome haben eine insgesamt bessere Prognose als nicht-epitheliale histologische Typen. Von Laborparameter haben sich niedrige Hämoglobinwerte, hohe Thrombozytenwerte und eine hohe LDH prognostisch ungünstig. Von den neuen Labormarkern sind zahlreiche in Evaluierung, wobei noch keine Daten für prognostische Werte vorliegen.
|
T- Status |
||
| T1 | ipsilaterale parietale Pleura | |
| T1a | keine viszerale Pleura | |
| T1b | viszerale Pleura | |
| T2 | ipsilaterale Lunge, Zwerchfell, viszerale Pleura konfluierend; mindestens ein Kriterium erfüllt:. konfluierender Tumor der viszeralen Pleura (einschließl. Fissuren). Infiltration in Zwerchfellmuskulatur. Infiltartion in das Lungenparenchym | |
| T3 | endothorakale Faszie, mediastinales Fett, Brustwand fokal, Perikard nicht-transmural; mindestens ein Kriterium erfüllt:
|
|
| T4 | außer der ipsilateralen Pleura besteht eine Tumorinfiltration
|
|
|
N- Status |
||
| N1 | LK- Metastasen ispilateral bronchopulmonal und / oder hilär | |
| N2 | LK- Metastasen subkarinal, ipsilateral an A. mammaria interna, und/ oder ipsilateral mediastinal | |
| N3 | LK- Metastasen kontralateral mediastinal, kontralateral an A. mammaria int., kontralateral hilär, ipsilateral in Skalenusgruppe / supraklavikulär und/ oder kontralateral in Skalenusgrupper / supraklavikulär | |
|
M- Status |
||
| M1 | Fernmetastasen | |
|
UICC Stadien (7. Auflage) |
|||
| IA | T1a | N0 | M0 |
| IB | T1b | N0 | M0 |
| II | T2 | N0 | M0 |
| III | T1, T2 | N1, N2 | M0 |
| T3 | N0, N1, N2 | M0 | |
| IV | T1, T2, T3 | N1 | M0 |
| T4 | jedes N | M0 | |
| jedes T | N3 | M0 | |
| jedes T | jedes N | M1 | |
Therapie
Chirurgische Therapie
Debulking/Pleurektomie
Hierbei handelt es sich um eine effektive aber nicht radikale Tumormassenreduktion mit makroskopischer Tumorentfernung, Das Tumordebulking kann eine gefangene Lunge, Thoraxwandinfiltrationen entfernen und dadurch eine Symptomkontrolle durch Beseitigung von Restriktion und Schmerzen.
Es gibt wenig Evidenz über die Prognose und Wertigkeit dieses Verfahrens und randomisierte Studien fehlen völlig. Einige Studiengruppen insbesondere in Großbrittanien erarbeiten weitere Daten insbesondere in Kombination mit chemischer Pleurodese. Kleinere Studien ergeben Hinweise auf gute Prognose mit tolerabler Morbidität.
Extrapleurale Pneumonektomie
Um eine komplette radikale Tumoroperation zu ermöglichen ist eine vollständige Tumormassenentfernung notwendig. Dies gelingt mittels einer extrapleuralen Pneumonektomie (EPP) mit en bloc Entfernung von Lunge, Pleura, Zwerchfell und Pericard sowie Entfernung sämtlicher Lymphknoten. Die EPP sollte an erfahrenen Zentren ausschließlich im Rahmen von multimodalen Therapien erfolgen. Die Mortalität der Operation konnte unter 5% gesenkt werden und das berichtete Overall Survival beträgt 12 – 24 Monate.
Eine EPP und ein multimodales Schema sollte in folgenden Situationen angedacht werden:
– Patient fähig sowohl für eine Pneumonektomie als auch für eine Chemotherapie und postoperative Radiatio
– Tumorstadium T1-3N0-1M0
– Tumor mit guter Prognose (epitheliales MPM, histologische verifiziert)
Chemotherapie
Generell sollte allen Patienten mit einem Performance Status > 2 eine palliative Chemotherapie angeboten werden. Zwar existiert nur eine einzige Placebo kontrollierte Studie zur Erstlinien Therapie des malignen Mesothelioms, die einen geringen Effekt zu Gunsten der Therapie mit Vinorelbin erbrachte. Die Empfehlungen einer Standardtherapie mit Cisplatin in Kombination mit einem modernen Antifolaten (Pemetrexed oder Ralitrexed) fußt auf zwei randomisierten Studien im Vergleich zu einer Cisplatin-Monotherapie (CIS + Pemetrexed und CIS + Ralitrexed). Obwohl hier keine Placebo kontrollierte Studie vorliegen und die Cisplatin Monotherapie nie gegenüber Placebo in einer randomisierten Studie verglichen wurde, sprechen die erreichten mittleren Überlebensraten von 12,1 Monaten im Vergleich zu untherapierten 6-9 Monaten für die Empfehlung einer Chemotherapie. Die Überlegenheit dieser Therapien konnten in insgesamt drei Studien nachgewiesen werden und zeigten bessere Ergebnisse als eine Cisplatin Monotherapie sowohl im Überleben als auch in der Remissionszeit. Auch anderen Kombinationstherapien Cisplatin + Etoposide, Methotrexat oder Interferon wurden getestet und in einer Metaanalyse zusammengefasst. Die Gesamtergebnisse erreichen die Überlebenszeiten der Antifolatkombinationen nicht. Die Kombination mit Pemetrexed wurde auch mit Carboplatin im Vergleich zu Cisplatin mit gleichen Ergebnissen getestet.
Für eine Secondline Therapie gibt es keine generelle Empfehlung, da wenig Datenmaterial in der Literatur verfügbar ist. Es gibt Hinweise auf ein besseres Überleben mit Chemotherapie versus ausschließlich Best supportive Care. Als Substanzen für die Secondline-Therapie stehen eine Pemetrexed Monotherapie, Vinorelbine Monotherapie (aufgrund der positiven first-line Daten als Monosubstanz) oder neuerliche Kombinationen zur Verfügung. Letztere allerdings ohne klaren Benefit für die Patienten.
Prinzipiell sollte eine Chemotherapie so rasch als möglich nach Diagnose begonnen werden. Im Falle einer multimodalen Therapie im Regelfall als Induktionstherapie vor einer geplanten radikalen Operation. Die Dauer einer Chemotherapie beträgt 4 – 6 Zyklen einer Erstlinien Therapie mit Cisplatin und Pemetrexed. Die Erfahrungen mit diesem Schema stammen aus der Behandlung des nicht-kleinzelligen Bronchuskarzinoms, wo eine Therapie von 4 Zyklen generell und sechs Zyklen nur bei gutem Ansprechen und fehlenden Grad 3 und 4 Toxitäten empfohlen werden.
Interleukine und Interferone wurden in Studien getestet, ebenso wie die Anwendung von zielgerichteten Therapien (targeted therapies) mit monoklonalen Antikörpern. In mehreren Studien wurden folgende Substanzen evaluiert:
– Thalidomide (negative Studie)
– Bevazizumab (kein Überlebensvorteil)
– Gefitinib
– Erlotinib
– Imatinib
Zahlreiche zytostatische und immunmodulierende Substanzen sind weiter in Erprobung.
Radiatio
Die Anwendung der Strahlentherapie ist in verschiedenen Situationen möglich. Erstens als Schmerztherapie bei lokaler Infiltration in Thoraxwandstrukturen zur Schmerzlinderung. Hier werden ähnliche Dosen wie bei anderen Tumoren mit Thoraxwandinfiltrationen empfohlen.
Bestrahlung der Operationskanäle nach Thorakoskopie und Drainagen
Insbesondere aufgrund einer französischen Studie wurde die Bestrahlung des OP-Kanals nach Thorakoskopien zur Verhinderung der Tumoraussaat entlang des Trokarkanales empfohlen. 3 x 7 Gy wurden lokal angewendet und verhinderten eine subkutane Tumoraussaat. Mehrere später durchgeführte Studien zeigten jedoch keinen Unterschied in der Überlebenszeit und auch nicht in der Anzahl der aufgetretenen Tumorrezidive im Drainagebereich. Diesbezüglich muss individuell entschieden werden. Im Rahmen von multimodalen Ansätzen sollten entweder das drainierte Areal mitbestrahlt oder entsprechend chirurgisch reseziert werden.
Postoperative Radiatio nach radikalen Operationen
Im Anschluss an eine Dekortikation/Pleurektomie sollte nach derzeitigem Stand keine Strahlentherapie erfolgen. Der zusätzliche Nutzen ist nicht bewiesen. Nach einer EPP sollte nur im Rahmen von multimodalen Konzepten eine Radiatio des gesamten Hemithorax mit 54Gy erfolgen. Die beschriebenen Rekurrensraten betragen zwischen 13 und 50%. Bei einer konventionellen Bestrahlung können wichtige Teile der Pleura aufgrund benachbarter Organa nicht ausreichend bestrahlt werden (Leber, Herz, große Gefäße im Mediastinum). Eine intensivierte modulierte Radiotherapie (IMRT) gibt die Möglichkeit organschonend eine hohe Strahlendosis auf die operierte Pleuragrenze zu applizieren, dafür wurden hohe Raten an Strahlenpneumonitis der kontralateralen Lunge. Diese Therapie kommt in multimodalen Studienkonzepten zur Anwendung und zeigt vielversprechende Ergebnisse.
Multimodale Therapie
Die Rationale für eine multimodale im Idealfall eine trimodale Therapie beruht auf der Tatsache, dass aufgrund der anatomischen Lokalisation eine kurative chirurgische Resektion nicht möglich ist. Alle Resektion müssen im onkologischen Sinn als R1 Resektionen gewertet werden. Ziel der chirurgischen radikalen Therapie ist eine makroskopische Tumorfreiheit der Thoraxhöhle zu erreichen. Der geforderte Abstand von 1 – 2 cm im gesunden Gewebe ist chirurgisch nicht möglich.
Die perkutane Radiatio ist durch die Organgrenzen und Toxizität in den Gesunden Organen limitiert. Zahlreiche Zentren sind auf die Kombination von Chemotherapie im adjuvanten Setting, gefolgt von radikaler Operation und anschließender perkutaner RT oder vermutlich besser IMRT übergegangen.
Auswahlkriterien für diese Verfahren sind:
- Klare histologische Sicherung des Tumors. Epitheliale MPM zeigen eine bessere Prognose.
- Radiologischer Ausschluss einer multinodulären Beteiligung mehr als N2, kontralateraler Befall der Thoraxhöhle, Befall des Peritoneums, Invasion unterhalb des Zwerchfells.
- Eine präoperative Lungenfunktion, die eine ausreichende postoperative Funktion der Restlunge ermöglichen
- Gute kardiale Funktion und bekannte Herzerkrankungen.
Seit längerem ist die Kombination von EPP mit Radiotherapie üblich. Zahlreiche vorwiegend nationale Studien kombinieren zusätzlich eine Induktionschemotherapie zu EPP + Radiotherapie. Zwei Studien wurden zwischenzeitlich präsentiert: die von der EORTC multizentrisch organisierte Studie mit 3 Zyklen Chemotherapie mit Cisplatin und Pemetrexed, folgend eine EPP und eine postoperative Radiatio mit 54Gy zeigte in der Phase II eine Vollremissionsrate von 42%, ein mittleres Gesamtüberleben von 18,4 Monaten und ein progression free survival (PFS) von mehr als 13 Monaten. Zahlreiche Arbeiten in unterschiedlichen Arbeitsgruppen wurden publiziert.
Palliation und Symptomenkontrolle
Die häufigsten Symptome beim Pleuramesotheliom sind Fatigue, Schmerzen, Husten, Atemnot und Gewichtsabnahme. Die rasche Progression und die schlechte Prognose erfordern eine gute palliative Behandlung der Patienten. Schmerztherapie erfolgt nach allgemeinen onkologische Kriterien und sollte insbesondere bei häufigen nervalen Schmerzen entsprechende Schmerzblockade und Neurolysetechniken miteinbeziehen.
Der Pleuraerguss stellte aufgrund der Häufigkeit ein wichtiges Symptom dar. Eine frühe Pleurodese kann lange das Wiederauftreten eines Ergusses verhindern. Multiple Punktionen sollten vermieden werden.
Eine allgemeine Palliation der Patienten zur Behandlung von Inappetenz, Übelkeit, Husten oder übermäßiges Schwitzen soll früh im Behandlungsprozess integriert werden. Bei vielen Patienten ist aufgrund des fortgeschrittenen Tumorprozesses der primäre therapeutische Ansatz eine gute Palliation.
Relevante Literatur
– ERS/ESTS Guidelines (2010)
– ESMO Guidelines (2010)
– IMIG Pathologie Guidelines (2012)